преподаватель, кафедра химии, Таласский государственный университет, г. Талас, Кыргызская Республика
Пищугин Федор Васильевич
доктор химических наук, профессор, Институт химии и химической технологии, член-корреспондент Национальной Академии Наук Кыргызской Республики, г. Бишкек, Кыргызская Республика
Тулебердиев Игорь Темерканович
кандидат химических наук, Институт химии и химической технологии, Национальная Академия Наук Кыргызской Республики, г. Бишкек, Кыргызская Республика
Основная биохимическая роль аскорбиновой кислоты в настоящее время сводится к окислительно-восстановительным биохимическим процессам. Однако, биохимическая роль витамина С, по-видимому, более многообразна. Так, например, сравнительно недавно в ряде исследований было обнаружено, что витамин С вместе с Fe (II) и О2 служит мощным не ферментативным гидроксилирующим реагентом для ароматических соединений. Как и гидролазы, этот реагент участвует в процессе превращения фенилаланина в тирозин. Имеется ряд работ по взаимодействию L-аскорбиновой кислоты с ароматическими аминами, фенилгидразином, никотинамидом [1]. Их можно отнести преимущественно к синтетическому профилю.
Представленное исследование посвящено изучению кинетики и механизма взаимодействия L- аскорбиновой и L-дегидроаскорбиновой кислот с никотинамидом, различными по структуре аминокислотами и ароматическими аминами. В литературе имеется большое количество трудов, посвященных изучению биохимической роли витаминов С и ее производных. Подавляющая часть работ занимается изучением их окислительно-восстановительных свойств при взаимодействии с различными химическими и биохимическими реагентами [2, 3]. Имеется небольшое количество научных исследований по синтезу продуктов взаимодействия L- аскорбиновой и L-дегидроаскорбиновой кислот с аминами, аминокислотами, йодом, диазометаном и другими реагентами, с целью установления структуры полученных продуктов [4, 5]. Витамины С, как показали наши исследования, имеют несколько реакционных центров в нуклеофильных реакциях, которые, как правило, протекают одновременно с образованием большого количества промежуточных и конечных продуктов. Выделение, очистка, установление их структуры представляют огромные трудности из-за низких выходов конечных продуктов и сложностью их разделения. Решение этих проблем можно осуществить только путем изучения кинетики и механизма этих реакций, расчетом их скорости и определения направления их протекания, определения энергетических, геометрических параметров исходных, промежуточных и конечных продуктов, выделения и идентификация их современными физико-химическими методами.
При недостатке витамина РР у детей развивается пеллагра, основными признаками которой является диарея (приводящая к истощению), деменция (нарушение психики и мышления) и в более тяжелых случаях – дерматит. Для профилактики гиповитаминоза витамин РР назначают детям, страдающим ахилией, энтеритами, колитами, аскоридозом, лямблиозом, язвенной болезнью, при которых нарушено всасывание витамина. С лечебной целью никотиновую кислоту или ее амид применяют для устранения авитаминоза и признаков гиповитаминоза; для ликвидации явлений гипоксии и ацидоза у детей с пневмониями, шоком, различными токсикозами, для стимуляции анаболических процессов при лечении гипотрофий, заболеваний печени [6].
Большой теоретический и практический интерес представляли синтез и изучение кинетики и механизма взаимодействия L-аскорбиновой кислоты с никотинамидом.
Для изучения взаимодействия L-аскорбиновой кислоты с аминокислотами использовалась аминокислоты (глицин, Д, L-α-аланин, β-аланин, L-лизин) производства венгерской фирмы «Reanal», а также отечественные препараты марки «х.ч.». За начало реакции был принят момент смешивания исходных растворов.
Методика эксперимента
Изучение кинетики и механизма конденсации L-аскорбиновой кислоты с аминами и аминокислотами показало, что скорости реакций их взаимодействия зависят от нескольких факторов: кето-ендиольного равновесия L-аскорбиновой кислоты, от основности и структуры нуклеофильного агента, катализатора и от условий проведения эксперимента.
Согласно данным [7], наибольшей реакционной способностью в L-аскорбиновой кислоте в реакциях нуклеофильного присоединения обладает С1-углеродный атом, поэтому присоединение нуклеофильного реагента протекает, прежде всего, по этому реакционному центру. Из двух таутомеров (енол- и кето-формы) наибольшей вероятностью присоединения аминов и аминокислот обладает дегидро-L-аскорбиновая кислота. Поэтому скорость присоединения аминов и аминокислот зависит от концентрации кето-формы, которая, в свою очередь, зависит от скорости перехода L-аскорбиновой кислоты в дегидро-L-аскорбиновую кислоту.
Скорость конденсации в целом складывается из скорости перехода L-аскорбиновой кислоты в дегидро-L-аскорбиновую кислоту (V1) и скорости взаимодействия дегидро-L-аскорбиновой кислоты с аминами и аминокислотами (V2):
Vконд=V1+V2
Как показали предварительные опыты при сливании растворов в результате взаимодействия компонентов появляется в начале розовая, а затем красная окраска, интенсивность которой со временем возрастает с появлением новых (нехарактерных для исходных веществ) максимумов поглощения в области 360 нм и 510 нм. Интенсивность их со временем увеличивается. Эквимолярные растворы L-аскорбиновой кислоты и аминокислот (глицин, Д, L-α-аланин, β-аланин, L-лизин) смешивались и выдерживались в течение 24 часов, при этом смеси окрашивались в интенсивно красный цвет. Растворы подвергались выпариванию при комнатной температуре. Выпавшие красные осадки перекристаллизовывались из пропанола.
Кинетика взаимодействия L-аскорбиновой кислоты с никотинамидом
В качестве объектов исследования были взяты L-аскорбиновая кислота и никотинамид марки «х.ч.». В качестве растворителя применялись водно-спиртовые буферные растворы, приготовленные по методике.
За начало реакции был принят момент смешивания растворов витамина С и никотинамида. Как показали предварительные опыты, при сливании термостатированных растворов в результате взаимодействия компонентов появляется желтая окраска и новый максимум поглощения в области 360 нм.
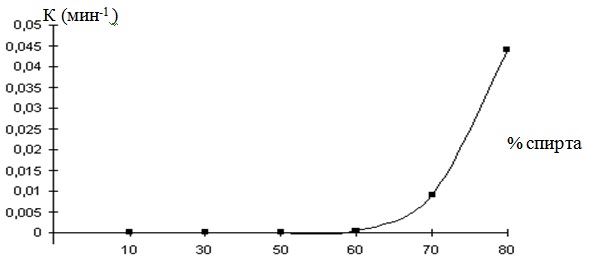
Рис.1. Зависимость константы скорости реакции от %-ного содержания спирта в водно-спиртовых буферных растворах (Т=200С)
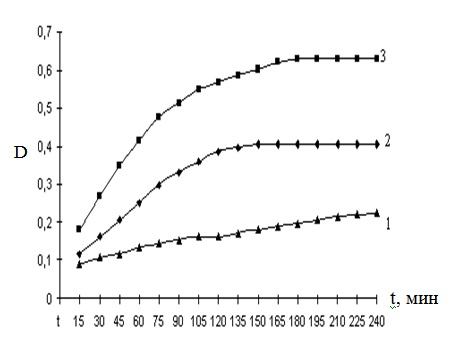
Рис.2. Кинетика взаимодействия L-аскорбиновой кислоты с никотинамидом при различных температурах в 70% буферном растворе (λ 360 нм, 1-200С, 2-300С, 3-400С)
Кинетика взаимодействия L-аскорбиновой кислоты с никотинамидом при различных температурах в 70% буферном растворе при λ 360 нм, показала, что энергия активации равна: Еакт=105,7 Дж/моль.
Таким образом, реакция взаимодействия L-аскорбиновой кислоты с аминокислотами, аминами и никотинамидом является в целом эндотермическим процессом [8].
Результаты изучения кинетики и механизма взаимодействия L-аскорбиновой кислоты с аминокислотами, аминами и никотинамидом показали, что процесс складывается из двух стадий:
- Стадии перехода L-аскорбиновой кислоты в дегидро-L-аскорбиновую кислоту.
- Стадии конденсации дегидро-L-аскорбиновой кислоты с аминокислотами, аминами и никотинамидом по С1-углеродному атому с образованием оснований Шиффа.
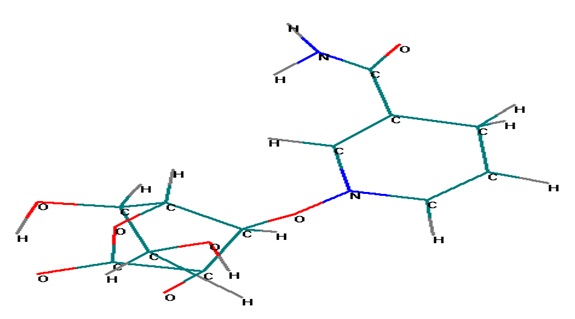
Рис.3. Продукт взаимодействия L-аскорбиновой кислоты с никотинамидом в хиноидной структуре.
Кинетика реакции взаимодействия аскорбиновой кислоты с аминокислотами
Взаимодействие L-аскорбиновой кислоты с аминокислотами имеет сложный характер из-за наличия в ней нескольких функциональных центров. L-аскорбиновая кислота характеризуется как довольно сильная кислота из-за наличия в ендиольной группировке двух ОН—-групп при С2 и С3 углеродных атомах. Причем, согласно литературным и нашим квантово-химическим расчетным данным, кислотные свойства ОН—-групп при С3 более сильные, чем кислотные свойства при С2 [9]. Поэтому при взаимодействии L-аскорбиновой кислоты с аминокислотами их аммонийные соединения, образующиеся за счет протонирования атома азота, имеющего свободную электронную пару, более предпочтительны за счет ОН—-группы при С3 по сравнению с ОН—-группой при С2. Эта реакция, по-видимому, протекает быстро. Однако здесь нужно учитывать, что в зависимости от структуры атакующего реагента и условий проведения реакций эти группы могут проявлять восстановительные свойства, если это возможно. На наш взгляд, было удивительно не учитывать реакционную способность карбонильной группы при С1 L-аскорбиновой кислоты. L-аскорбиновую кислоту общепризнанно относят к классу углеводов, в которых ОН—-группа при С1 является наиболее реакционно способной по сравнению с другими ОН—-группами в реакциях нуклеофильного замещения. По-видимому, многообразие и уникальность химии и биохимии этих витаминов объясняется их возможностью реагировать с различными реагентами по нескольким реакционным центрам и условиям их взаимодействия.
Как показали предварительные опыты при сливании растворов в результате взаимодействия компонентов появляется в начале розовая, а затем красная окраска, интенсивность которой со временем возрастает с появлением новых (нехарактерных для исходных веществ) максимумов поглощения в области 360 нм и 510 нм, интенсивность которых со временем увеличивается. Эквимолярные растворы L-аскорбиновой кислоты и аминокислот (глицин, Д, L-α-аланин, β-аланин, L-лизин) смешивались и выдерживались в течение 24 часов, при этом смеси окрашивались в интенсивно красный цвет. Растворы выпаривались при комнатной температуре. Выпавшие красные осадки перекристаллизовывались из пропанола [10].
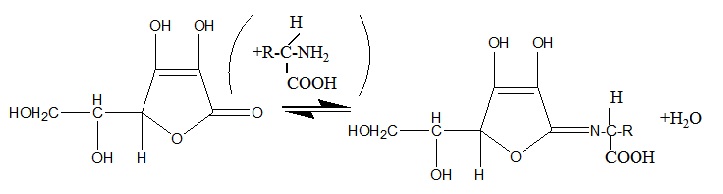
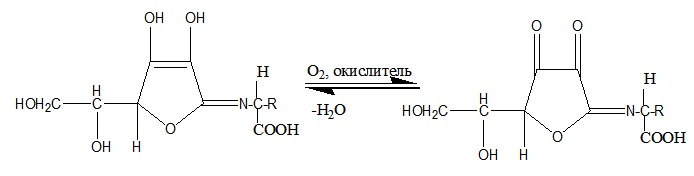
Как показали наши исследования, взаимодействие L-аскорбиновой кислоты в отсутствии в реакционных растворах кислорода воздуха или окислителей с аминокислотами преимущественно протекает по С1 –углеродному атому, имеющему большой положительный заряд на этом реакционном центре с образованием бесцветных оснований. Схема этих химических превращений оснований Шиффа представлена на рис. 4.
Рис.4. Взаимодействие L-аскорбиновой кислоты с аминокислотами
Рис.5. Окисление оснований Шиффа кислородом воздуха или окислителями
Обсуждение результатов: Квантово-химическая оценка реакционной способности витаминов С с азотосодержащими органическими соединениями
Анализ данных, полученных из научной литературы, показал, что L-аскорбиновая и дегидро- L-аскорбиновая кислоты, обладая несколькими реакционными центрами, могут взаимодействовать с большим числом азот-, серо-, кислородсодержащими соединениями. Скорость и направления путей взаимодействия этих реакций зависят от многих факторов:
1) структуры витаминов L-аскорбиновой и дегидро-L-аскорбиновой кислот; 2) энергетических и геометрических параметров реагирующих молекул; 3) величин зарядов на реакционных центрах витаминов С и атакующих реагентов; 4) пространственных факторов субстратов и реагентов; 5) внешних условий (температура, растворитель, рН-среды).
Для целенаправленного синтеза продуктов взаимодействия витаминов С с различными веществами, увеличения чистоты и выхода конечных продуктов необходимо методами кинетики провести изучение влияния каждого из этих факторов на скорость и направление протекания реакций. С помощью компьютерной программы ChyperChem методом ММДОЗ нами определены энергетические и геометрические параметры, заряды на узловых реакционных центрах витаминов С, и реагентов, а также продуктов возможных их химических превращений.
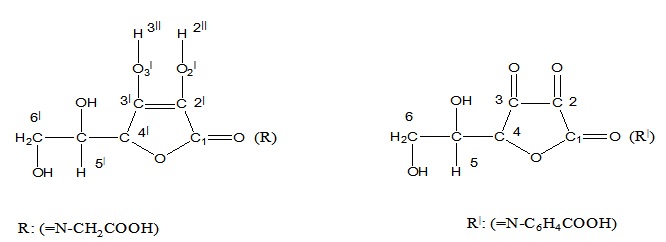
Рис.6. L-аскорбиновая и дегидро-L-аскорбиновая кислоты
Структуры полученных соединений доказаны методами элементного анализа. Однако эти работы были проведены без учета современных представлений и возможностей использования современных физико-химических и компьютерных методов. Нами была произведена критическая оценка взаимодействия обеих форм витамина С с нуклеофильными реагентами. Рассмотрим влияние каждого из условий на вероятность и пути протекания реакций нуклеофильного присоединения и замещения, с учетом определения энергетических, геометрических параметров, величин зарядов на узловых реакционных центрах:
- По энергетике и геометрическим параметрам, представленных в таблице оба витамина близки друг другу.
- а) Величины зарядов на возможных реакционных центрах (С1, С2 и С3) резко отличаются друг от друга.
Наибольшей вероятностью к нуклеофильной атаке имеют С1 (0,788 в L-аскорбиновой кислоте и 0,723 в дегидро-L-аскорбиновой кислоте), т.е. по реакционной способности три атома углерода располагаются в ряд С1>С3>С2. По кислотным свойствам гидроксилы при С3 –ОН Н (0,265) более кислые их по сравнению с С2-ОН Н (0,247), поэтому вероятность солеобразования с азотсодержащими реагентами у атома водорода при С3 будет несколько больше по сравнению с атомом водорода при С2. Это подтверждается и величинами положительных зарядов на С3 (0,403) и С2 (0,312) атомах углерода. Вероятность нуклеофильной атаки в дегидро-L-аскорбиновой кислоте по С3 и С2-углеродным, атомам, будет выше по сравнению с C2 и С3 L-аскорбиновой кислоты. б) Чем больше отрицательный заряд (рКа реагента), тем большая вероятность протекания реакций взаимодействия двух форм витамина С с азотсодержащими реагентами.
- Влияние пространственных факторов играет большую роль на скорость и направление протекания химических процессов. Анализ рассмотрения структур двух форм L-аскорбиновой кислоты на компьютерных и модельных образцах показал, что реакционный центр при С1 обладает более благоприятными пространственными возможностями для его нуклеофильной атаки по сравнению с С3 и С2. У L-аскорбиновой кислоты ОН-группа при С5 препятствует присоединению нуклеофила по С3, а в дегидро-L-аскорбиновой кислоте возникает препятствие со стороны кето-группы при С2 и ОН-группы при С5.
- Условия проведения реакций (рН-среды, температура, растворитель) нуклеофильного присоединения и замещения оказывают в ряде случае огромное влияние на скорости, механизм и направление протекания реакций. Результаты проведенных нами кинетических измерений показали [11,12], что в слабокислых и нейтральных средах в отсутствии кислорода воздуха и окислителей реакции взаимодействия L-аскорбиновой кислоты с азотсодержащими нуклеофильными реагентами протекает по С1 –реакционному центру с образованием оснований Шиффа. В присутствии кислорода воздуха или следов окислителя происходит окисление гидроксильных групп L-аскорбиновой кислоты с образованием системы сопряженных связей, при этом растворы окрашиваются в красный цвет с λмах 350 и 510 нм. Щелочные среды и повышенные температуры способствуют разрушению витаминов С с образованием многих промежуточных и конечных продуктов.
Таким образом, для целенаправленного получения новых соединений взаимодействия L-аскорбиновой и дегидро-L-аскорбиновой кислот c азотсодержащими реагентами, для снижения затрат, времени, увеличения чистоты и выхода конечных продуктов необходимо учитывать все представленные в работе параметры проведения реакций.
Список использованных источников
- Wenner W. The reaction of L-ascorbic and D-isoascorbic acid with nicotinic acid and its amide / W. Wenner // J. Org. Chem. – 1949. – V.14. – P. 22–25.
- Baile C. W. A Study of the Binary System Nicotinamide – Ascorbic Acid / C. W. Baile, I. R. Bricht, I. I. Iasper // J. Am. Chem. Soc. – 1945. – V. 67. – P. 1184.
- Романчук П. С. Стабилизирующее действие магния на аскорбиновую кислоту / П. С. Романчук // Доклады АН СССР. – 1957. – T.117. – С. 665–
- Khadem H. Studies On Dehydro-L-Ascorbic Acid Arylozasones / Н. Khadem, S. Ashry // J. Am. Chem. Soc. – 1968. – P. 2247–
- Синтез и превращения фосфитов 5,6-О-изопропилиден-L-аскорбиновой кислоты / Д. А. Предводителев, М. А. Маленковская, А. Р. Беккер, Л. К. Васянина, Э. Е. Нифантьев // Журнал органической химии. – 1991. –Т. 27. –В. 8. – С. 1655–
- Штамм Е. В. Катализ окисления аскорбиновой кислоты ионами Си2+ / Е. В. Штамм, А. П. Пурмаль, Ю. И. Скурлатов // Журнал физической химии. – 1974. – № 9. – С. 2233–
- Березовский В. М. Химия витаминов / В. М. Березовский. – М. : Пищевая промышленность, – С. 19–57.
- Пищугин Ф. В. Влияние среды на скорости взаимодействия L-аскорбиновой кислоты с аминокислотами / Ф. В. Пищугин, Б. Д. Сарыбаева // Наука и новые технологии. – 2006. –№1. – С. 149–152.
- Пищугин Ф. В. Влияние среды на скорости гидролиза продукта конденсации L-аскорбиновой кислоты с аминокислотами / Ф. В. Пищугин, Б. Д. Сарыбаева // Вестник КНУ им. Ж. Баласагына. – 2007. –Т.1, сер.5, вып.1. –С. 284–287.
- Иванов В. Г. Практикум по органической химии / В. Г. Иванов, О. Н. Гева, Ю. Г. Таверова. – М. : Академа, 2002. – 18 с.
- Сарыбаева Б. Д. Биологическая роль модифицированных витаминов С, РР, Н1 / Б. Д. Сарыбаева, Ф. В. Пищугин // Сб. статей по материалам 59 междунар. науч.-практ. конф. «Инновации в науке». –2016. – №2 (51). – С. 207–212.
- Сарыбаева Б. Д. Окислительно-восстановительные превращения продуктов взаимодействия аскорбиновой кислоты с азотсодержащими органическими соединениями / Б. Д. Сарыбаева, Ф. В. Пищугин // Символ науки. – 2016. – №3/2016. – Ч.4. – С. 49–53.
Sarybayeva Baktygul
teacher, Department Chemistry, Talas State University
Talas, Kyrgyz Republic
Pishchugin Fedor
Doctor of Chemistry, Professor, Institute of Chemistry and Chemical Technologies, Corresponding Member of National Academy of Sciences of the Kyrgyz Republic, Bishkek, Kyrgyz Republic
Tuleberdiev Igor
Doctor of Chemistry, Institute of Chemistry and Chemical Technologies, Corresponding Member of National Academy of Sciences of the Kyrgyz Republic, Bishkek, Kyrgyz Republic
KINETICS AND THE MECHANISM OF INTERACTION OF L-ASCORBIC ACID WITH NITROGEN-CONTAINING ORGANIC COMPOUNDS
The kinetics and the mechanism of interaction L-ascorbic and L-dehydroascorbic of acids with Nicotinamidum, amino acids are studied. Methods of synthesis of products of interaction and condensation of L-ascorbic acid with Nicotinamidum, amino acids, amines are developed; their structures are established by modern physical and chemical methods (an ultimate analysis, UF-, IK-spectroscopies, TSH, a polarimetry). Results of the conducted researches can be used as models in biochemical processes with participation of vitamins C, as new biologically active medicinal and vitamin preparations in medicine, in veterinary science, agriculture.
Keywords: kinetics, mechanism, interaction, Nicotinamidum, amino acid, amines, structure, method, polarimetry, spectroscopy, elemental analysis.
© АНО СНОЛД «Партнёр», 2017
© Сарыбаева Б. Д., 2017
© Пищугин Ф. В., 2017
© Тулебердиев И. Т., 2017